2022年1月22日/医麦客新闻 eMedClub News/--近年来,全球已有多款CAR-T产品获批上市,用于治疗不同类型的血液系统恶性肿瘤。CAR-T在血液瘤领域一路高歌猛进,而在患者人群占比超90%以上的实体瘤领域,CAR-T疗法则进展缓慢,困难重重。
为克服CAR-T在实体瘤中的局限性,来自意大利IRCCS圣拉斐尔科学研究所的科学家们,发现了肿瘤细胞表面的一种“屏障”,而用2-脱氧葡萄糖(2-Deoxyglucose,2DG)破坏这层结构则能够增强CAR-T对实体瘤的杀伤能力。这项研究在近日发表于SCIENCE TRANSLATIONAL MEDICINE杂志。

这种屏障是一种被称为N-聚糖的糖基化结构,可以保护肿瘤免受CAR-T细胞的杀伤。
糖基化是最常见的蛋白质修饰之一,而肿瘤细胞往往会表现出异常的糖基化。与健康细胞相比,肿瘤细胞表面的聚糖表达更加多样化;其中,N-聚糖的增加是肿瘤中最常见的变化之一。因此,N-聚糖可作为抗肿瘤治疗的一个新靶点。
为了验证这一点,圣拉斐尔的研究人员首先在胰腺癌细胞中敲除了MGAT5基因,来生成N-糖基化缺陷型模型(MGAT5基因编码一种合成N-聚糖的关键酶);再利用CAR-T细胞对N-糖基化缺陷胰腺肿瘤细胞进行处理。
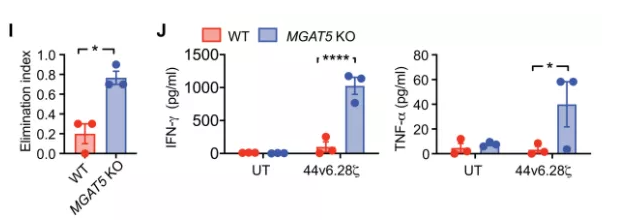
结果表明,削弱胰腺肿瘤中N-聚糖的合成确实能够改善CAR-T细胞的抗肿瘤活性,使细胞溶解活性、细胞因子IFN-γ和TNF- α的水平增加。
▲ 削弱N-聚糖合成显著增强了CAR-T细胞的抗肿瘤功效
(图片来源:SCIENCE TRANSLATIONAL MEDICINE)
通过深入研究疗效背后的机制,研究人员还发现N-聚糖还干扰了免疫突触的形成,而CAR依靠这种免疫突触来激活T细胞并发挥其功能;因此,去除N-聚糖可提高免疫突触质量并改善CAR信号传导。
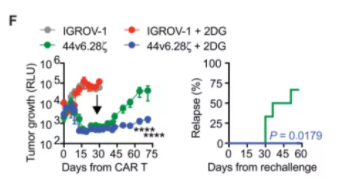
为此,该团队尝试用葡萄糖类似物2DG来阻断N-聚糖。在两种胰腺癌异种移植小鼠模型中,2DG和CAR-T细胞的组合使用表现出显著的肿瘤控制,且相比于2DG或CAR-T细胞的单独使用,显著延长了小鼠的生存期。
▲ 2DG糖基化阻断显著增强CAR-T抗实体瘤效果
(图片来源:SCIENCE TRANSLATIONAL MEDICINE)
更重要的是,在接受2DG处理的小鼠中,肿瘤中T细胞的耗竭特征减少,同时TIM-3、PD-1等几种免疫扼制标志物的表达降低。该结果表明,2DG可能有效地解决了T细胞耗竭的问题,这也是当前CAR-T用于实体瘤面临的主要障碍之一。
除了胰腺癌之外,2DG还有助于改善CAR-T在其它高度糖基化肿瘤中的杀伤力,包括膀胱癌、卵巢癌等。
总体而言,研究发现在CAR-T对抗实体瘤的过程中,N-聚糖通过干扰免疫突触形成,减少转录激活、细胞因子的产生并降低细胞毒性,来保护肿瘤免受CAR-T细胞杀伤。为克服这一障碍,利用葡萄糖类似物2DG破坏肿瘤细胞上的N-聚糖“屏障”,可提高CAR-T在胰腺癌、膀胱癌等高度糖基化肿瘤中的杀伤力,还可以帮助CAR-T细胞逃避免疫检查点扼制。
该研究团队认为,通过改善CAR-T细胞活化和减轻细胞耗竭,打破肿瘤细胞表面的糖屏障是克服CAR-T治疗实体瘤局限的一种有前景的策略。
下一代CAR-T细胞疗法前沿进展
CAR-T细胞治疗实体瘤的障碍是复杂且多因素的,其局限性包括:缺乏肿瘤特异性靶标、免疫扼制性肿瘤微环境、肿瘤浸润不良等。为克服这些挑战,下一代CAR-T疗法的开发目前已形成两种主要趋势:一种是将CAR-T细胞与其他疗法联用(包括“武装”抗癌药物),另一种是优化CAR-T本身。
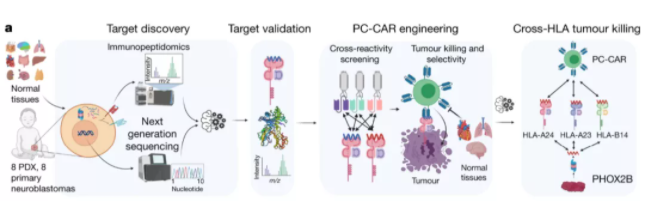
➤ 为了解决缺乏肿瘤特异性抗原的问题,2021年11月3日,Nature杂志发表了一项宾夕法尼亚大学费城儿童医院的新研究,题为“Cross-HLA targeting of intracellular oncoproteins with peptide-centric CARs”。研究团队设计了“以肽为中心”的CAR-T细胞(PC-CAR T),该疗法能够通过识别呈现在肿瘤细胞表面上的肽,来靶向肿瘤细胞内的关键蛋白来消除肿瘤。
对于实体瘤来说,大多数负责肿瘤生长和生存的蛋白都存在于肿瘤细胞的细胞核中,而不是细胞表面,因此CAR-T细胞往往无法接触。相反,癌细胞也可以将细胞内蛋白呈现在MHC上,如果所呈现的是突变的肽,也将可能被CAR-T识别。
▲ 图片来源:Nature
➤ 针对CAR-T细胞耗竭问题,2021年12月2日,宾夕法尼亚大学医学院的Carl June团队发表在Cell上的一篇题为“An NK-like CAR T cell transition in CAR T cell dysfunction”的论文,揭示了CAR-T的可塑性,并证明了ID3和SOX4表达的基因下调可以预防或延迟CAR-T细胞耗竭,从而提高实体瘤CAR-T细胞治疗的疗效。
▲ 图片来源:Cell
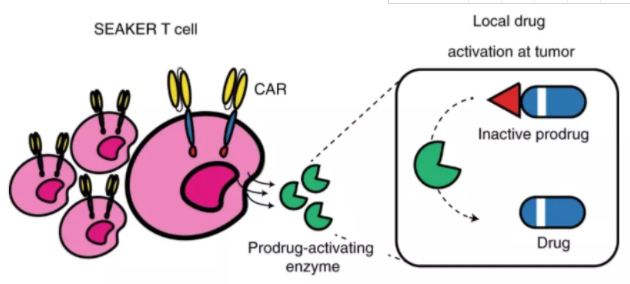
➤ 同样克服T细胞耗竭难题,2021年12月30日,Nature Chemical Biology杂志发表了一篇题为“Engineering CAR-T cells to activate small-molecule drugs in situ”的研究,纪念斯隆-凯特琳癌症中心(SKI)的科学家们开发出了一种新的CAR-T细胞——SEAKER 细胞(synthetic enzyme-armed killer cells,合成酶武装杀伤细胞)。
这些细胞可以直接向肿瘤输送杀伤性抗癌药物,既杀死含有癌症标志物的肿瘤细胞,也能杀死不含癌症标志物的癌细胞。更重要的是,SEAKER细胞即使在耗竭的情况下也能继续产生抗癌药物,并且这种药物不会被癌细胞抑制。
▲ 图片来源:Nature Chemical Biology
参考资料:
1.https://www.fiercebiotech.com/research/stop-sugarcoating-cancer-cells-to-empower-car-t-therapy-solid-tumors
2.https://www.science.org/doi/10.1126/scitranslmed.abg3072
该文章来自于网络转载,版权归原作者所有。如有涉及侵权请给予告知,我们将尽快删除相关内容。