
CAR-T虽然在血液肿瘤疗效惊艳,目前已有5款产品上市。但对于实体瘤,从目前发表的公开的临床数据看,响应率依然非常低。本文简要梳理目前实体瘤CAR-T开发前10位的靶点及临床概况(超过总临床数量的60%),供大家参考。
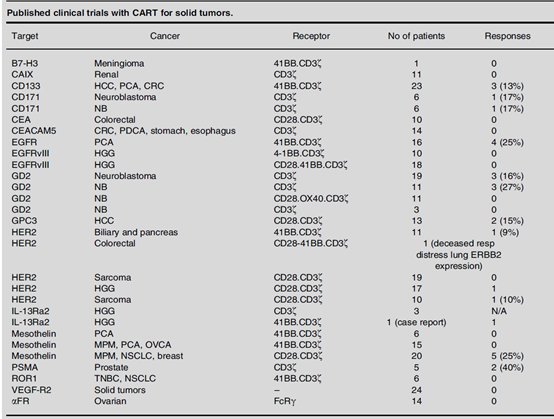
Current Opinionin Pharmacology 2021, 59:70–84
1.Mesothelin
靶点简介
间皮素,各种实体肿瘤中过表达,在健康间皮细胞中有限表达,是一种比较理想的TAA,on- target, off- tumour毒性小。
临床概况
可以检索到29项临床试验,实体瘤排名第一。如上图所示,单一治疗的临床疗效有限,响应率不超25%。
2.GD2
靶点简介
双唾液酸神经节苷脂GD2在正常组织中的表达主要局限于中枢神经系统、周围感觉神经纤维、真皮黑素细胞、淋巴细胞和间充质干细胞。正常细胞生理功能尚未完全阐明。在癌症中,GD2有助于增强肿瘤细胞的增殖、运动、迁移、粘附和侵袭、抵抗凋亡。
临床概况
可以检索到26项临床试验,排名第二。如上表所示,单一治疗的临床疗效有限。
3.HER2
靶点简介
HER2的致癌潜力已在多种人类恶性肿瘤中得到证实,尤其是在乳腺癌、胃癌、胃食管交界处癌等。在这些癌症中,HER2激活的主要机制是HER2基因扩增,导致HER2蛋白在细胞膜上完全过表达。此外HER2的基因突变也是关键因素之一。
临床概况
同样可以检索到26项临床试验,作为一个经典靶点,抗体药物和ADC药物都取得了的临床突破,但是CAR-T细胞临床试验疗效有限。
4.GPC3
靶点简介
GPC3由580个氨基酸组成的65kD蛋白,在健康胎儿的肝脏和肾脏中表达,但在成人中很少表达,除了胎盘。但是在多种肿瘤中表达,肝细胞癌(HCC)、卵巢透明细胞癌、黑色素瘤、肺癌鳞状细胞癌、肝母细胞瘤、肾母细胞瘤(Wilms瘤)、卵黄囊瘤和一些儿童癌症。GPC3是实体瘤非常理想的靶点,基于此,多种免疫治疗(包含CAR-T)在开发。
临床概况
可以检索到23项临床试验。
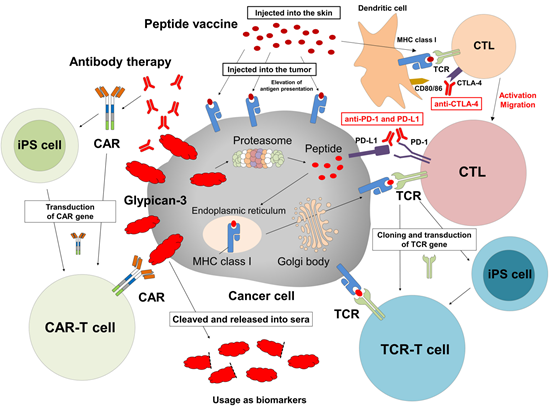
Front.Oncol. 9:248
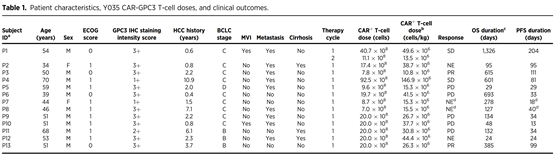
仁济医院及科济药业2020年在Clin Cancer Res发表了临床试验(NCT02395250,NCT03146234)结果,13例病人,根据Kaplan-Meier方法,3年、1年和6个月的总生存率分别为10.5%、42.0%和50.3%。1例病情持续稳定的患者在44.2个月后存活。CAR-T细胞的扩增往往与肿瘤反应呈正相关。
5.Claudin18.2(CLDN18.2)
靶点简介
CLDN18.2是膜上皮紧密连接蛋白Claudin18(CLDN18)的剪接变体,已被鉴定为一种很有前途的靶向的生物标志物。CLDN18.2在正常组织中的表达谱受限,仅在胃粘膜紧密连接的超分子复合物中表达。而在恶性转化后,细胞极性的变化导致CLDN18.2表位的暴露,适用于靶向治疗。除胃癌外,CLDN18.2在各种原发肿瘤和转移癌中异常表达,包括胰腺癌、胆道癌、卵巢癌和肺腺癌。
临床概况
可以检索到10项临床试验。
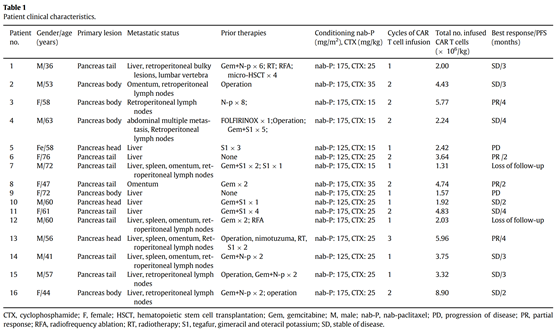
科济药业自主研发的CT041在中国启动了针对晚期(不可切除或转移性)胃癌/胃食管结合部癌和胰腺癌的Ib/II期临床试验(NCT04581473),在美国启动了针对晚期(不可切除或转移性)胃癌或胰腺癌的Ib期临床试验( NCT04404595)。
2021年欧洲肿瘤内科学会大会(2021 ESMO)进行口头报告,36例具有肿瘤靶病灶的患者中,31例患者观察到不同程度的目标病灶缩小,总客观缓解率(ORR)为48.6%,疾病控制率(DCR)为73.0%。
6.CEA
靶点简介
癌胚抗原(carcinoembryonic antigen,CEA)1965年由Gold和Freedman首先从结肠癌和胚胎组织中提取的一种肿瘤相关抗原,是一种广谱肿瘤标志物。针对CEA CAR-T理论上具有广谱抗癌效果。
临床概况
可以检索到10项临床试验,单一治疗的临床试验中显示疗效有限。
NCT02416466,CAR-T Hepatic Artery Infusionsand Sir-Spheres for Liver Metastases (HITM-SIR),RogerWilliams Medical Center.
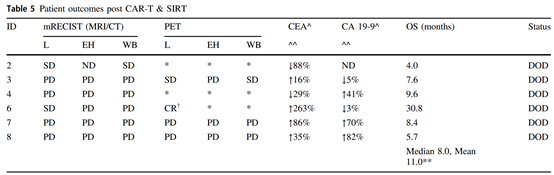
NCT02349724,AClinical Research of CAR T Cells Targeting CEA Positive Cancer,Southwest Hospital, China
7.EGFRvIII
靶点简介
EGFRvIII是EGFR最常见的突变,不存在于正常组织,发生在25-64%的胶质母细胞瘤。EGFRvIII增强肿瘤发生,增加肿瘤细胞运动能力,对化疗等产生耐药。
临床概况
可以检索到11项临床,2项由Gary Archer Ph.D., Duke University注册的临床(NCT03283631,NCT02664363),因为经费等已经终止。NCT02209376终止,改为联合治疗。目前尚有8项临床在开展。
由National CancerInstitute (NCI) 的Steven Rosenberg, M.D 开展的NCT01454596,结果发表,患者基本无应答。

8.PSMA
靶点简介
前列腺特异性膜抗原(PSMA)是一种II型膜糖蛋白,作为前列腺癌的肿瘤相关抗原在前列腺癌领域被研究了30年。
临床概况
目前有10项临床试验注册,其中6项来自于深圳市免疫基因治疗研究院。目前尚未有公开的文献发表相关临床数据。
CAR-T大佬Carl H. June基于前期研究,注册了NCT03089203(CART-PSMA-TGFβRDN Cells forCastrate-Resistant Prostate Cancer)。在其临床前研究论文中评论了,由MemorialSloan Kettering Cancer Center进行的临床研究(NCT01140373)“自2010年以来,该anti-PSMA CART,持久性有限,没有观察到患者应答”(文献6)。
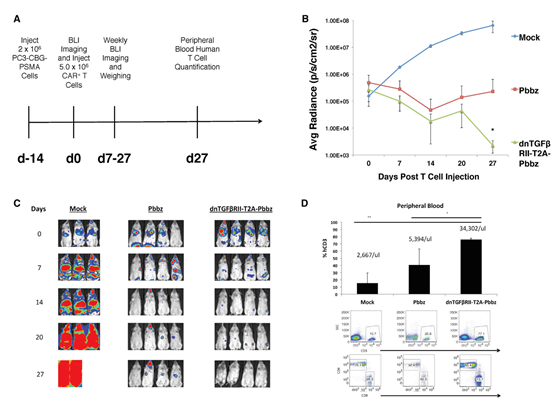
CART-PSMA-TGFβRDN小鼠模型数据(文献6)
9.EGFR
靶点简介
EGFR是一种I型跨膜蛋白,具有细胞质酪氨酸激酶活性,属于HER/ErbB家族,在大约40-89%的NSCLC中过表达,并在NSCLC的进展中发挥着重要作用。此外EGFR也在胰腺癌等恶性实体瘤高表达。
临床概况
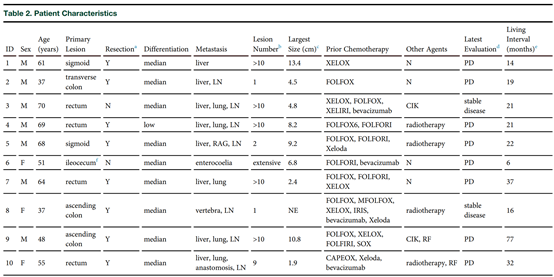
有10项临床注册,显示出一定临床效果。

NCT03182816 CTLA-4 andPD-1 Antibodies Expressing EGFR-CAR-T Cells for EGFR Positive Advanced SolidTumor,上海细胞治疗研究院。结果:9例病人,1例PR,6例SD,2例PD。(文献7)
NCT01869166,Treatment of Chemotherapy RefractoryEGFR(Epidermal Growth Factor Receptor) Positive Advanced Solid Tumors(CART-EGFR) (CART-EGFR),解放军总医院韩卫东教授。(文献8)
结果:16例病人,4例PR,8例SD。
10.EpCAM
靶点简介
上皮细胞粘附分子(Epithelial cell adhesion molecul,EpCAM)是一种跨膜糖蛋白,主要在某些管腔上皮细胞上以有序定向表达。在恶性转化后,EpCAM在一些癌细胞上以不受限制的模式过表达。
临床概况
目前有9项临床注册,来自于国内华西医院、安徽省立第二医院、安徽医科大学第一医院。
目前,尚无公开发表数据。
小结
实体瘤CAR-T目前有约40个靶点进入临床试验,其中前10个靶点占据了总临床数量的60%以上。从目前临床数据看,HER2、GD2等经典靶点并没有观察到良好的临床应答,Claudin18、GPC3等靶点,显示了一定的临床应答。实体瘤CAR-T面临的几大问题,肿瘤局部浸润困难、持久性差、肿瘤微环境的生存低等,依然制约着CAR-T在实体瘤临床的发展。
近几年,将细胞因子基因工程入CAR-T以增加持久性、生存能力、功能;通过基因编辑去除免疫检查点;以及采用肿瘤浸润淋巴细胞(TIL)等,取得了一些进展,但依然需要在临床试验中进行检验。
参考文献
1.Victor Moreno et al,Adoptive cell therapy for solid tumors:Chimeric antigen receptor T cells and beyond,CurrentOpinion in Pharmacology 2021, 59:70–84
2.Mount, C. W. et al. Potent antitumor efficacy of anti-GD2 CAR T cells in H3-K27M+ diffuse midline gliomas. Nat. Med.24,572–579 (2018).
3.Shimizu Y, Suzuki T, YoshikawaT, Endo I and Nakatsura T (2019) Next-Generation Cancer Immunotherapy TargetingGlypican-3. Front. Oncol. 9:248
4. DonghuaShi et al,ChimericAntigen Receptor-Glypican-3 T-Cell Therapy for Advanced HepatocellularCarcinoma: Results of Phase I Trials,Clin Cancer Res .2020 Aug 1;26(15):3979-3989.
5. StevenC. Katz et al,HITM-SIR:phase Ib trial of intraarterial chimeric antigen receptor T-cell therapy andselective internal radiation therapy for CEA+ liver metastases,Cancer Gene Therapy https://doi.org/10.1038/s41417-019-0104-z
6. ChengchengZhang et al,Phase IEscalating-Dose Trial of CAR-T Therapy Targeting CEA+ Metastatic ColorectalCancers, Molecular Therapy Vol. 25 No 5 May 2017
7. ChristopherC. Kloss et al,Dominant-NegativeTGF-b Receptor Enhances PSMA-Targeted Human CAR T Cell Proliferation AndAugments Prostate Cancer Eradication,Molecular TherapyVol. 26 No 7 July 2018
8. YajunZhang et al,Phase Iclinical trial of EGFR‑specifcCAR‑T cells generated by thepiggyBac transposon system in advanced relapsed/refractory non‑small cell lung cancer patients,Journal of Cancer Researchand Clinical Oncology https://doi.org/10.1007/s00432-021-03613-7
9. YangLiu et al,Anti-EGFRchimeric antigen receptor-modified T cells in metastatic pancreatic carcinoma:A phase I clinical trial,Cytotherapy 22 (2020) 573-580
该文章来自于网络转载,版权归原作者所有。如有涉及侵权请给予告知,我们将尽快删除相关内容。